Sisältö
- Tärkein ero
- Protonaatio vs. protonisaatio
- Vertailutaulukko
- Mikä on protonointi?
- Mikä on protonointi?
- Keskeiset erot
- johtopäätös
Tärkein ero
Tärkein ero protonaation ja deprotonoitumisen välillä on se, että protoneinti on protonin lisääminen kemialliseen yhdisteeseen, kun taas deprotonointi on protonin eliminointia kemiallisesta yhdisteestä.
Protonaatio vs. protonisaatio
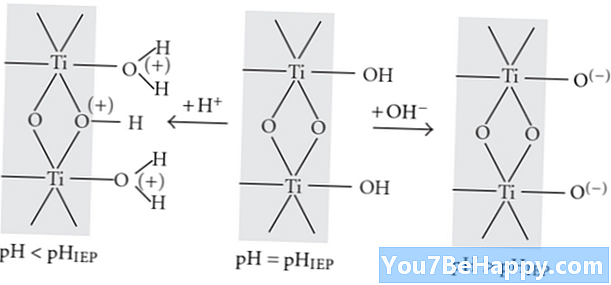
Protonointi on kemiallinen prosessi, joka tapahtuu kemiallisten reaktioiden aikana, joissa protoni lisää kemialliseen yhdisteeseen; toisaalta deprotonointi on prosessi, joka tapahtuu kemiallisen reaktion aikana, jossa protoni poistuu kemiallisesta yhdisteestä. Protonointi on +1-varauksen lisäys atomissa, molekyylissä, ionassa tai yhdisteessä; toisaalta, deprotonointi on atomin, ionin, molekyylin tai yhdisteen +1-varauksen vähenemistä.
Protonaatioon osallistuvaa atomia, molekyyliä tai yhdistettä kutsutaan emäkseksi; kääntöpuolella atomia, molekyyliä tai yhdistettä, joka osallistuu deprotonointiin, kutsutaan hapoksi. Protonointi on prosessi, jossa kemiallisen yhdisteen pH nousee; päinvastoin, deprotonointi on prosessi, jossa kemiallisen yhdisteen liuoksen pH laskee.
Protonointi on additioprosessi, kun taas deprotonointi on prosessin poistamista tai eliminointia. Protonointi on kemiallinen prosessi, jossa kemiallisissa reaktioissa lisätty energia; kääntöpuolella; deprotonointi on kemiallinen prosessi, jossa reaktioiden aikana vapautuva energia. Toisin sanoen protonaatio on H: n lisäys+ kemiallisessa yhdisteessä; ja toisaalta deprotonointi on H: n poistamista+ kemiallisesta yhdisteestä.
Protonointi lisää atomin, ionin tai molekyylin varausta; kääntöpuolella deprotonointi vähentää ionin, atomin tai molekyylin varausta. Emäksissä tapahtuu protonaation kemiallisia prosesseja aina happo-emäs-reaktioiden aikana; toisaalta hapot suoritetaan aina prototisoinnin kemiallisissa prosesseissa happo-emäs-reaktioiden aikana.
Protonointi on kemiallinen menetelmä konjugaattihappojen tuottamiseksi kemiallisten prosessien aikana; kääntöpuolella; deprotonointi on kemiallinen prosessi konjugaatin emäksen tuottamiseksi kemiallisen prosessin aikana. Protonisaatio aiheuttaa aina vesimolekyylien tuotannon yhdisteen hydroksyyliryhmistä kemiallisissa prosesseissa; kääntöpuolella deprotonoituminen aiheuttaa aina hydroksyylimolekyylien tuotannon vesimolekyyleistä kemiallisissa prosesseissa.
Protonointi on erittäin nopea kemiallinen prosessi orgaanisten reaktioiden aikana; toisaalta deprotonointi on erittäin hidas prosessi orgaanisten reaktioiden aikana. Protonointi on kemiallinen prosessi, joka stimuloi isomerointiprosessia, kun taas kemiallinen prosessi, joka stimuloi isomerointiprosessia. Protonointi on lisääntyvä happamuuden luonne; kääntöpuolella deprotonointi on perusmerkin kasvava nopeus.
Vertailutaulukko
| protonaatio | deprotonoitumisen |
| Protonointi on protonin lisääminen kemialliseen yhdisteeseen. | Deprotonointi on protonin eliminointia kemiallisesta yhdisteestä. |
| protoneja | |
| Protonit lisäävät yhdisteeseen | Protonit poistuvat yhdisteestä |
| Charge | |
| Se lisää molekyylin +1-varausta | Se vähentää molekyylin +1 varausta |
| Happamuusaste tai emäksisyys | |
| Perusteellisuusaste | Happamuusaste |
| Yhdisteen pH | |
| Se nostaa yhdisteen pH: ta | Se alentaa yhdisteen pH: ta |
| Prosessin nopeus | |
| Se on nopea prosessi | Se on hidas prosessi |
| Isomerointiprosessi | |
| Stimuloi isomerointiprosessia | Inhiboi isomerointiprosessia |
| Prosessin energia | |
| Se lisää energiaa reaktioon | Se vapauttaa energiaa reaktioista |
| Prosessin tyyppi | |
| Lisäysprosessi | Prosessin poistaminen |
| H+ Ioni | |
| Vetyioneja lisätään yhdisteeseen | Vetyionit poistuvat yhdisteestä |
| palautuvuudesta | |
| Se on palautuva prosessi | Se on peruuttamaton prosessi |
| Katalyyttinen kyky | |
| Sillä on katalyyttinen voima | Sillä ei ole katalyyttistä voimaa |
Mikä on protonointi?
Protonointi on kemiallinen prosessi, jossa kemiallisiin yhdisteisiin lisätään protonia kemiallisten reaktioiden aikana. Se on erittäin nopea prosessi. Se voi muodostaa vesimolekyylejä hydroksyylimolekyyleistä. Protonointi on palautuva prosessi, joka lisää kemiallisen yhdisteen varausta +1 varauksen nopeudella atomissa, ioneissa, molekyyleissä tai lajeissa.
Protonointiin osallistuvien liuosten tai liuottimien pH on erittäin alhainen. Protonointi on kemiallisten tai orgaanisten yhdisteiden emäksisyyden tai happamuuden määrä. Protonointi on additio- tai endoterminen prosessi, joka osallistuu isomerointiprosessiin. Se myös stimuloi polymerointiprosessia.
Sillä on katalyyttinen voima lisätä niiden reaktioiden happamuutta, joita käytetään useissa prosesseissa, kuten additioreaktioissa, nukleofiilisissä, elektrofiilisissä reaktioissa, substituutioreaktioissa jne. Protonimisprosessi on verrannollinen aineen happamuusluokkaan. Siihen sisältyy yleensä vesimolekyylien muodostuminen prosessin aikana.
Vetyioneja lisätään aina kemialliseen yhdisteeseen protoniprosessin aikana. Sillä on myös kyky muuttaa molekyylin optisia ominaisuuksia. Yhdisteiden protonointiprosessi riippuu liuosten tai liuottimien käytettävissä olevien happojen happamuusasteesta. Protonointiprosessia käytetään vähentämään orgaanisten molekyylien reaktiivisuutta. Protonisaatio tunnetaan yleensä endotermisenä prosessina, johon sisältyy energian vapauttaminen luovuttamalla protoni kemiallisille lajeille erittäin helposti.
Prosessi, kuten vedyn lisääminen ammoniakkimolekyyliin, joka johtaa ammoniumionien muodostumiseen, vetyionien lisääminen vesimolekyyleihin hydroniumionien tuottamiseksi, hydroksyyli-ionien protonointi vesimolekyylien muodostamiseksi, vetyionien lisääminen alkoholien kanssa hydroniumionien muodostamiseksi liuoksessa, vetyionien lisääminen alkeeniin ja alkyeneihin jne. selittää parhaiten termin protonaatio.
Mikä on protonointi?
Deprotonointi on kemiallinen prosessi protonien poistamiseksi kemiallisista yhdisteistä kemiallisten reaktioiden aikana. Se on hidas prosessi. Tällä prosessilla on myös kyky muodostaa hydroksyyli-ioneja vesimolekyyleistä. Deprotonointi on peruuttamaton prosessi, jolla on kyky vähentää kemiallisen yhdisteen varausta +1 varauksen nopeudella atomissa, molekyylissä tai ionilajeissa.
Deprotonointiprosessiin osallistuvien liuosten tai liuottimien pH on erittäin korkea. Tällä prosessilla ei ole kykyä suorittaa kemiallisia reaktioita toimimalla katalysaattorina. Protonisaatioprosessi on verrannollinen aineen perusominaisuuteen. Vetyionit poistuvat kemiallisesta yhdisteestä aina protonisointiprosessin aikana. Sen optiset aktiivisuudet ovat myös muuttuvat.
Deprotonointimenetelmä riippuu myös liuosten tai liuottimien pH: sta. Tämä prosessi lisää orgaanisten molekyylien reaktiivisuutta. Prosessit, kuten vetyionien poistaminen vedestä hydroksyyli-ionien muodostamiseksi, protonin poistaminen alkaanista alkeenien ja alkyenien muodostamiseksi, vetyionien poisto alkoholista jne., Selittävät parhaiten termin deprotonointi.
Keskeiset erot
- Protonaatio on protonin lisäyksen ilmiö; toisaalta deprotonointi on protonin poiston ilmiö.
- Protonointi nostaa aina kemiallisen liuoksen pH: ta; kääntöpuolella deprotonoituminen laskee aina kemiallisen liuoksen pH: ta.
- Protonointi lisää aina +1-varauksen kemialliseen yhdisteeseen; Toisaalta deprotonointi poistaa aina +1-varauksen kemialliselle yhdisteelle.
- Protonointi on lisääntyvä happamuuden luonne; kääntöpuolella deprotonointi on perusmerkin kasvava nopeus.
- Protonointi tapahtuu erittäin nopeasti; toisaalta deprotonointi tapahtuu hyvin hitaasti.
- Emäkset, joita yleensä käytetään protonaatioprosessissa hyväksymällä protoni; päinvastoin; deprotonointi, jota yleensä käytetään deprotonointiprosessissa poistamalla protonit.
- Energian lisäys tapahtuu protonaatioprosessissa; kääntöpuolella, energian poisto tapahtuu protonisointiprosessissa.
- Protonointi lisää atomin, ionin tai molekyylin varausta; kääntöpuolella deprotonointi vähentää ionin, atomin tai molekyylin varausta.
- Protonointiprosessiin sisältyy kemiallisten aineiden isomerointi; toisaalta deprotonointiprosessi ei sisällä kemiallisten aineiden isomerointia.
- Protonointi on kemiallinen prosessi, joka tapahtuu emäksissä happo-emäs-reaktioiden aikana; kääntöpuolella deprotonointi on kemiallinen prosessi, joka tapahtuu hapoissa happo-emäs-reaktioiden aikana.
- Protonointi tuottaa konjugaattihapon aina kemiallisessa prosessissa; päinvastoin, deprotonointi tuottaa aina konjugaattiemäksen kemiallisessa prosessissa.
- Protonointi tekee liuoksesta väkevämmän; kääntöpuolella deprotonoituminen tekee liuoksesta vähemmän konsentroituneen.
- Protonointi liittyy vesimolekyylien valmistukseen; toisaalta deprotonointi käsittää hydroksyylimolekyylien valmistuksen.
- Protonointi on endoterminen prosessi; toisaalta deprotonointi on eksoterminen prosessi.
johtopäätös
Yllä olevasta keskustelusta päätellään, että protonaatio on kemiallisen yhdisteen +1-varauksen lisäys; toisaalta deprotonointi on kemiallisen yhdisteen +1-varauksen vähenemistä.